Bakterien
Die mikrobiologische Untersuchung mit dem Lichtmikroskop ist fester Bestandteil der Aufgaben in einem medizinischen Labor. Ziel der Untersuchung ist die Suche und der Nachweis von Infektionserregern in Patientenproben. Zu den Infektionserregern zählen Pilze, Viren, Parasiten und Bakterien. Manche Bakterien können schwere Krankheiten wie zum Beispiel Pest und Cholera auslösen. Daher ist deren Nachweis essentiell, um daraus Hinweise auf die Therapie des infizierten Patienten abzuleiten. Bakterien sind kleine, einzellige Mikroorganismen, die im Durchschnitt zwischen 0,5 – 10 Mikrometer groß sind. Sie lassen sich anhand ihrer Morphologie gut mit dem Mikroskop nachweisen. Bakterien liegen unter anderem in Stäbchenform, Kugelform (Kokken), Fadenform oder Spirillenform (Spirochäten) vor (Abb. 1). Bakterien haben zwar ein kernäquivalentes Genom (Nukleoid), besitzen jedoch keinen Zellkern (Prokaryoten) und in der Regel keine Organellen. Bakterienchromosomen bestehen aus den größten zirkulären DNA-Molekülen der Bakterien und schwimmen frei im Zytoplasma der Zelle. Im Zytoplasma finden sich weitere kleine DNA-Moleküle, die meist ringförmig und doppelsträngig vorliegen und Plasmide genannt werden. Diese zählen nicht zu den Chromosomen und können von einem Bakterium zu einem anderen übertragen werden.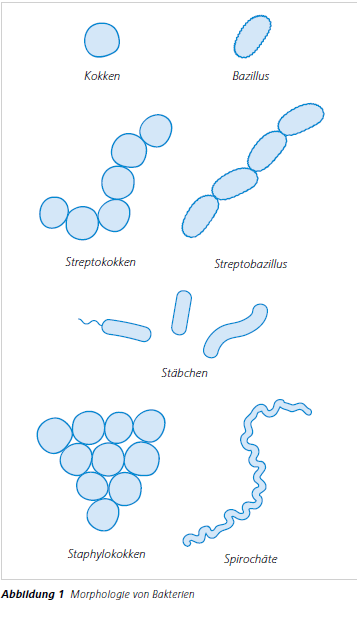
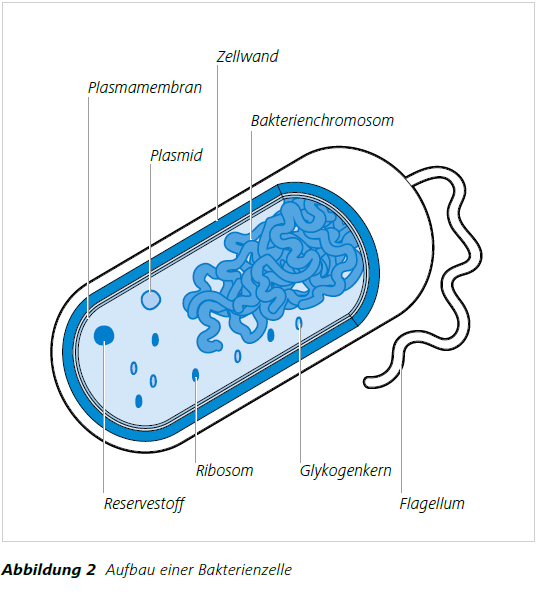 Ribosome werden bei der Translation im Rahmen der Proteinbiosynthese benötigt. Um das Zellplasma liegt die Plasma- bzw. Zellmembran, die für den Austausch von Stoffen zwischen dem Inneren und Äußeren der Zelle sorgt. Außerhalb der Plasmamembran befindet sich die Zellwand, die dafür sorgt, dass die Zelle ihre Form behält. Sie schützt auch vor einem Konzentrationsaustausch mit der Umgebung, der durch den osmotischen Druck zu Stande käme und die Zelle zum Platzen bringen würde. Um die Zellwand befindet sich eine Schleimschicht, die die Bakterien vor dem Austrocknen schützen. Außen an der Zelle befinden sich viele Pili (Zellfortsätze). Sie können zum Beispiel an Feststoffen, an Nahrung aus der Umgebung oder an anderen Bakterien anheften. Eine Vielzahl der Bakterien besitzen ein Flagellum. Dieses auch Geißel genannte fadenförmige Gebilde aus Proteinen dient der Fortbewegung (Abb. 2). Bakterien vermehren sich durch Zellteilung. Eine Zelle verdoppelt ihre Organellen, um sich danach in zwei Teile zu teilen. Es entstehen zwei identische Zellen mit dem gleichen Genom.
Ribosome werden bei der Translation im Rahmen der Proteinbiosynthese benötigt. Um das Zellplasma liegt die Plasma- bzw. Zellmembran, die für den Austausch von Stoffen zwischen dem Inneren und Äußeren der Zelle sorgt. Außerhalb der Plasmamembran befindet sich die Zellwand, die dafür sorgt, dass die Zelle ihre Form behält. Sie schützt auch vor einem Konzentrationsaustausch mit der Umgebung, der durch den osmotischen Druck zu Stande käme und die Zelle zum Platzen bringen würde. Um die Zellwand befindet sich eine Schleimschicht, die die Bakterien vor dem Austrocknen schützen. Außen an der Zelle befinden sich viele Pili (Zellfortsätze). Sie können zum Beispiel an Feststoffen, an Nahrung aus der Umgebung oder an anderen Bakterien anheften. Eine Vielzahl der Bakterien besitzen ein Flagellum. Dieses auch Geißel genannte fadenförmige Gebilde aus Proteinen dient der Fortbewegung (Abb. 2). Bakterien vermehren sich durch Zellteilung. Eine Zelle verdoppelt ihre Organellen, um sich danach in zwei Teile zu teilen. Es entstehen zwei identische Zellen mit dem gleichen Genom.
Gramfärbung
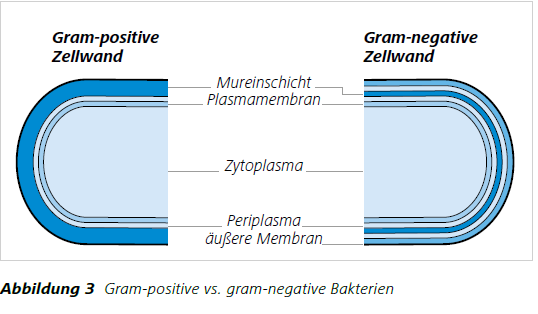
Die Gramfärbung [1] ist eine vom dänischen Bakteriologen Hans Christian Gram (1853 – 1938) entwickelte Methode zur differenzierenden Färbung von Bakterien für die mikroskopische Untersuchung. Diese Färbemethode basiert auf dem damals unbekannten Unterschied im Zellwandaufbau von Bakterien, da die unterschiedliche Färbbarkeit der Bakterien auf deren chemischen und physikalischen Eigenschaften basiert.Es werden gram-positive und gram-negative Bakterien unterschieden. Allerdings können nicht alle Bakterienarten durch diese Technik klassifiziert werden. Es gibt auch gram-variable und gram-unbestimmte Arten. Die meisten Bakterien nutzen in Ihrem Aufbau der Zellmembran ein Makromolekül (Peptidoglykan) als einhüllendes und strukturgebendes Gerüst. Dieses Molekül bezeichnet man als Murein. Murein ist ausgesprochen stabil und bedingt durch seine unterschiedlichen Ausprägungen die Morphologie der meisten Bakterien [2]. Bedingt durch die Dicke der Mureinschicht kann man die zwei prinziellen bakteriellen Bauformen unterscheiden. Gram-positive Bakterien haben eine dicke Zellwand, die hauptsächlich aus einer bis zu 40 Schichten, 15 – 80 nm dicken Lage Murein bestehent. Die gram-negativen Bakterien besitzen nur eine 10 – 20 nm dünne Wand aus einer ein bis wenigschichtigen Lage Murein. Außerdem haben sie eine zweite Lipidmembran ähnlich einer Cytoplasmamembran außerhalb der Zellwand (Abb. 3).
Ablauf der Gramfärbung (Abb. 4)
Die zu färbenden Bakterien werden auf einen Objektivträger aufgetragen, getrocknet und anschließend zwei bis drei Minuten mit dem Farbstoff Kristallviolett angefärbt. Kristallviolett ist ein positiv geladener Anilinfarbstoff. Das Präparat wird kurz mit destilliertem Wasser abgespült und im Anschluss ca. eine Minute mit Lugolscher Lösung (Iod-Kaliumiodid- Komplex) behandelt. Dadurch bildet sich in den Mureinschichten ein Farbstoff-Iod-Komplex. Das Präparat wird wiederholt mit destilliertem Wasser abgespült. Der Farbkomplex ist wasserunlöslich. Im nächsten Schritt folgt die eigentliche Differenzierung.
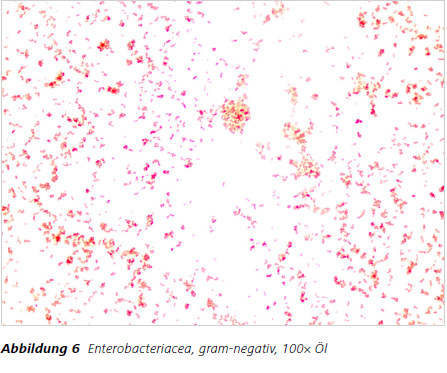
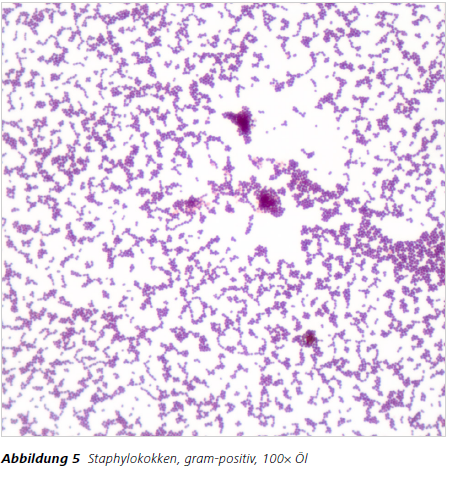
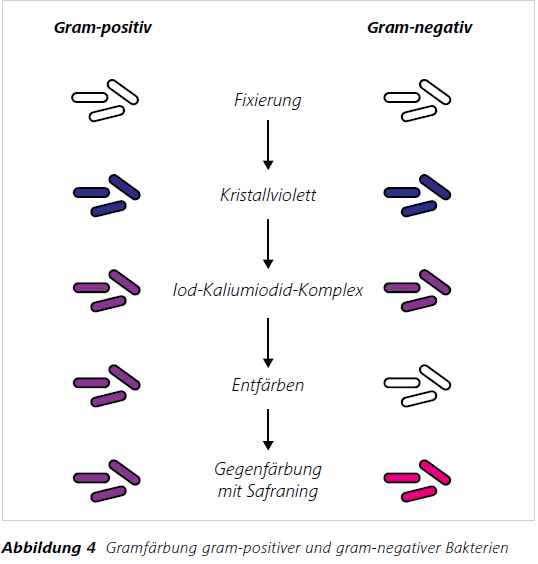 Dazu wird das Präparat in der Differenzierungslösung (96 % Alkohol) geschwenkt, bis keine Farbwolken mehr abgegeben werden. Gram-positive Bakterien lassen sich durch diese Differenzierung nicht so leicht entfärben, da der Farbstoff-Iod-Komplex sehr stabil in den Mureinschichten haftet und der Alkohol nicht durch die dicke Zellwand der gram-positiven Bakterien dringen kann. Gram-negative Bakterien lassen sich im Gegensatz dazu relativ leicht mit Alkohol entfärben. Durch die anschliessende einminütige Gegenfärbung mit Safranin werden die gramnegativen Bakterien gemarkert, worauf sie rot beziehungsweise rot-orange (Abb. 5 und Abb. 6) erscheinen.
Dazu wird das Präparat in der Differenzierungslösung (96 % Alkohol) geschwenkt, bis keine Farbwolken mehr abgegeben werden. Gram-positive Bakterien lassen sich durch diese Differenzierung nicht so leicht entfärben, da der Farbstoff-Iod-Komplex sehr stabil in den Mureinschichten haftet und der Alkohol nicht durch die dicke Zellwand der gram-positiven Bakterien dringen kann. Gram-negative Bakterien lassen sich im Gegensatz dazu relativ leicht mit Alkohol entfärben. Durch die anschliessende einminütige Gegenfärbung mit Safranin werden die gramnegativen Bakterien gemarkert, worauf sie rot beziehungsweise rot-orange (Abb. 5 und Abb. 6) erscheinen.
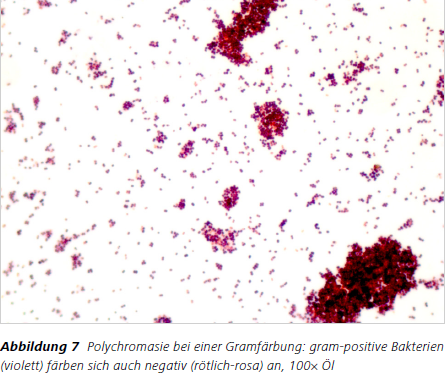
 Die Gramfärbung ist bei korrekter Durchführung sehr aussagefähig und eine schnelle Methode, unterschiedliche Bakterien zu differenzieren. Die korrekte Durchführung beinhaltet unter anderem, dass bei der Differenzierung nur die gram-negativen Bakterien komplett entfärbt werden. Dies erreicht man durch die optimale Zeitdauer der Differenzierung. Bei zu kurzer Differenzierung bleiben auch die gram-negativen Bakterien mit kristallviolett angefärbt. Differenziert man dagegen zu lange, entfärben sich sowohl die gram-negativen als auch die gram-positiven Bakterien. Ein Testpräparat zur Überprüfung der korrekten Anfärbung ist zu empfehlen [2].
Die Gramfärbung ist bei korrekter Durchführung sehr aussagefähig und eine schnelle Methode, unterschiedliche Bakterien zu differenzieren. Die korrekte Durchführung beinhaltet unter anderem, dass bei der Differenzierung nur die gram-negativen Bakterien komplett entfärbt werden. Dies erreicht man durch die optimale Zeitdauer der Differenzierung. Bei zu kurzer Differenzierung bleiben auch die gram-negativen Bakterien mit kristallviolett angefärbt. Differenziert man dagegen zu lange, entfärben sich sowohl die gram-negativen als auch die gram-positiven Bakterien. Ein Testpräparat zur Überprüfung der korrekten Anfärbung ist zu empfehlen [2].
Systematik der Bakterien nach Verhalten in der Gramfärbung

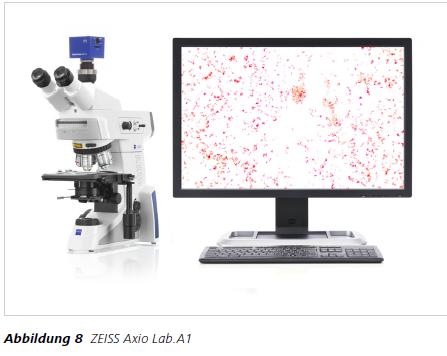
Empfohlene Mikroskop-Ausstattung
Gramgefärbte Bakterien werden mit einem Durchlichtmikroskop im Hellfeld betrachtet (Abb. 8). Zur mikroskopischen Visualisierung der kleinen Bakterien ist ein Objektiv mit hoher Apertur und hoher Endvergrößerung erforderlich, erreichbar mit einem 100× Ölobjektiv wie z.B. ZEISS N-Achroplan.Da es bei der Identifikation auf die sichere Differenzierung von Blau / Violett- zu Rottönen ankommt, ist auf eine gute Farbkorrektur der eingesetzten Objektive zu achten. Das Kürzel „Achro“ weist im Namen des Objektives auf diese Korrektur hin. Ein Objektiv kann seine volle Leistungsfähigkeit erst dann entwickeln, wenn auch der Kondensor diese Farbkorrektur leistet, wie z.B. ZEISS #424225-9070-000 achromatisch – aplanatischer Kondensor. Zur Dokumentation der Bilder ist eine Mikroskopkamera mit gutem Dynamikumfang zu empfehlen.
Zusammenfassung
Durch geeignete, differenzierende Färbungen lassen sich Bakterien im medizinischen Labor mithilfe eines Lichtmikroskops bestimmen und unterscheiden. Die Gramfärbung ist eine der geläufigsten Färbemethoden, mit deren Hilfe Bakterien auf einfache Art und Weise anhand des Aufbaus ihrer Zellwand unterschieden werden können. Zu einer sicheren Interpretation ist eine sorgfältige Präparation und eine hochaperturige Optik mit hoher Endvergrößerung zu benutzen.Quellennachweise:
[1] https://de.wikipedia.org/wiki/Gram-F%C3%A4rbung
[2] Maria Mulisch, Ulrich Welsch (Hrsg.). Romeis Mikroskopische Technik, 18. Auflage 2010, S. 243f.
[3] Dörries, Hof. Medizinische Mikrobiologie, Thieme Verlag, 6. Auflage 2014, S. 284ff.